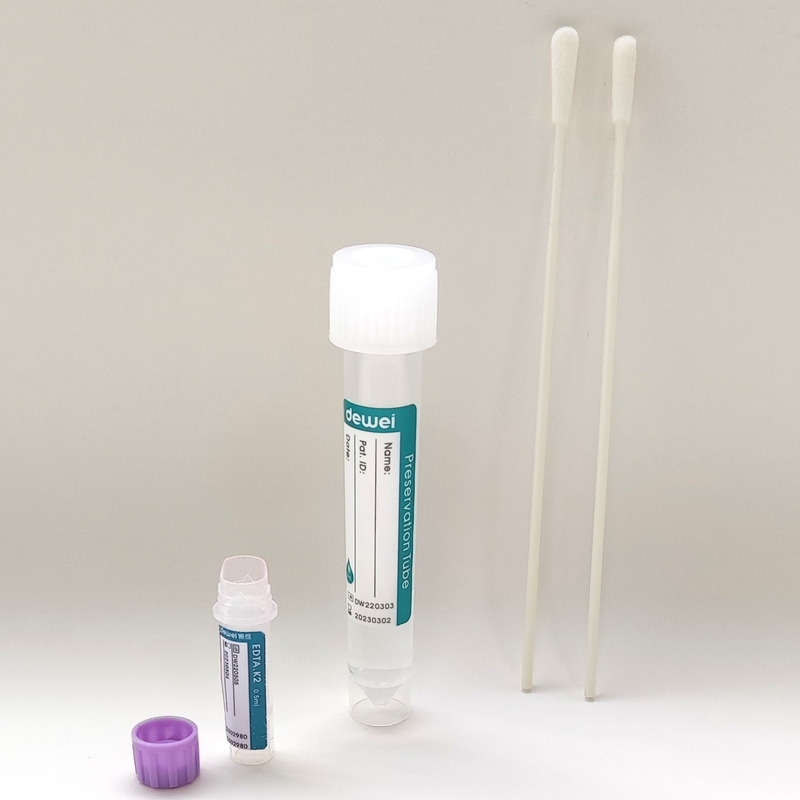
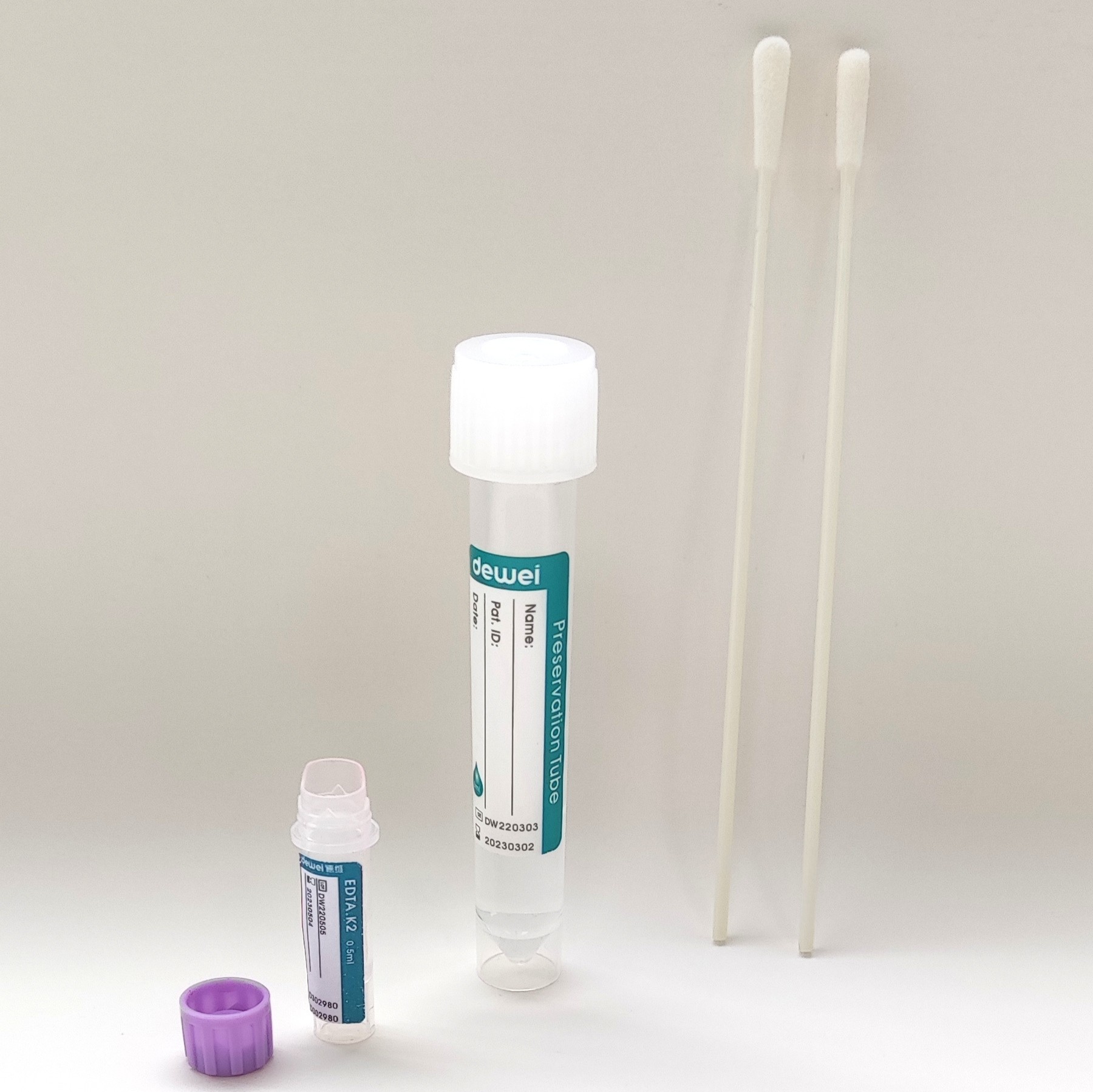
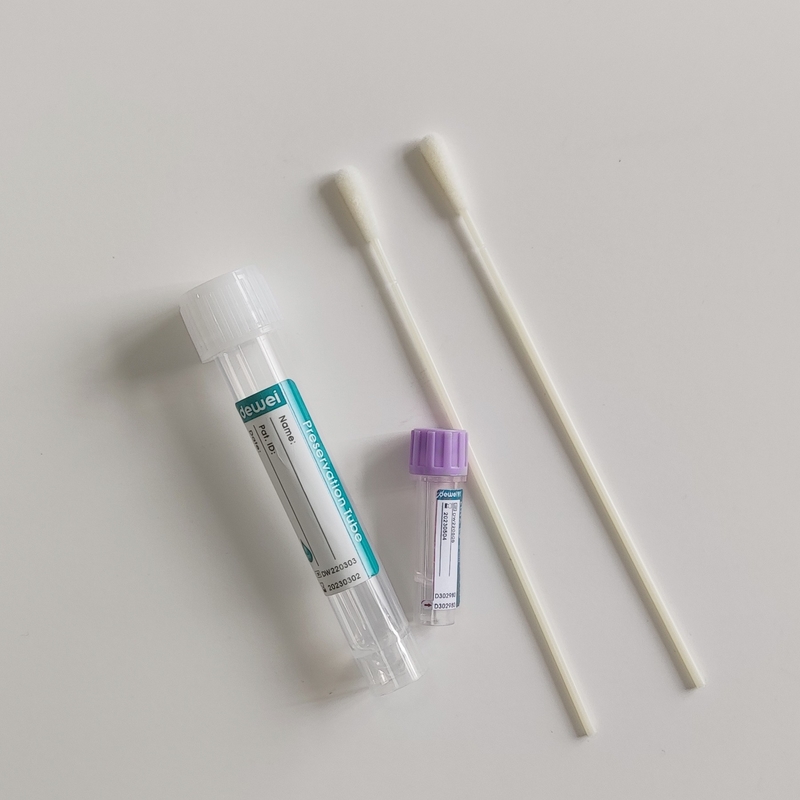
ชุดตรวจหากรดนิวคลีอิก Monkeypox Virus (วิธี Fluorescence PCR)
[ข้อมูลจำเพาะ]
24tests/kit, 48tests/kit, 96tests/kit
[ตั้งใจใช้]
ชุดนี้ใช้เพื่อตรวจหาคุณภาพ DNA ของไวรัส Monkeypox ที่สกัดจากตัวอย่างเลือด เซรั่ม หรือ lesion exudate ของผู้ป่วยที่ต้องสงสัยว่าติดเชื้อและผู้ป่วยรายอื่นที่ต้องวินิจฉัย
[หลักการ]
ชุดนี้ใช้เทคโนโลยี PCR เรืองแสงแบบเรียลไทม์เพื่อเลือกบริเวณที่มีการอนุรักษ์ของชิ้นส่วนกรดนิวคลีอิกของไวรัส Monkeypox เป็นพื้นที่เป้าหมายการขยายพันธุ์ ออกแบบไพรเมอร์เฉพาะและฉลากโพรบเรืองแสงที่แตกต่างกัน และใช้เทคโนโลยี RT-PCR เพื่อตรวจหาว่าตัวอย่างมีไวรัส Monkeypox หรือไม่ ดีเอ็นเอ.
[ส่วนประกอบ]
| ข้อมูลจำเพาะ |
ส่วนประกอบ |
บรรจุุภัณฑ์ |
วัตถุดิบ |
| 24การทดสอบ/ชุด |
MPV PCR รีเอเจนต์ A |
408μL×1 หลอด |
ไพรเมอร์เฉพาะ โพรบ บัฟเฟอร์กรดทริส-ไฮโดรคลอริก ฯลฯ |
| MPV PCR รีเอเจนต์ B |
72μL×1 หลอด |
เอ็นไซม์ Taq แบบ Hot-start, uracil-N-glycosylase เป็นต้น |
| MPV Positive Control |
400 ไมโครลิตร×1 หลอด |
ลำดับดีเอ็นเอที่มียีนเป้าหมาย |
| MPV ลบการควบคุม |
400 ไมโครลิตร×1 หลอด |
NaCl |
| 48การทดสอบ/ชุด |
MPV PCR รีเอเจนต์ A |
816μL×1 หลอด |
ไพรเมอร์เฉพาะ โพรบ บัฟเฟอร์กรดทริส-ไฮโดรคลอริก ฯลฯ |
| MPV PCR รีเอเจนต์ B |
144μL×1 หลอด |
เอ็นไซม์ Taq แบบ Hot-start, uracil-N-glycosylase เป็นต้น |
| MPV Positive Control |
400 ไมโครลิตร×1 หลอด |
ลำดับดีเอ็นเอที่มียีนเป้าหมาย |
| MPV ลบการควบคุม |
400 ไมโครลิตร×1 หลอด |
NaCl |
| 96การทดสอบ/ชุด |
MPV PCR รีเอเจนต์ A |
816μL×2 หลอด |
ไพรเมอร์เฉพาะ โพรบ บัฟเฟอร์กรดทริส-ไฮโดรคลอริก ฯลฯ |
| MPV PCR รีเอเจนต์ B |
หลอด 144μL×d |
เอ็นไซม์ Taq แบบ Hot-start, uracil-N-glycosylase เป็นต้น |
| MPV Positive Control |
400 ไมโครลิตร×2 หลอด |
ลำดับดีเอ็นเอที่มียีนเป้าหมาย |
| MPV ลบการควบคุม |
400 ไมโครลิตร×2 หลอด |
NaCl |
บันทึก:
ห้ามผสมส่วนประกอบจากแบตช์ที่ต่างกันสำหรับการตรวจจับ
รีเอเจนต์การสกัดกรดนิวคลีอิก: แนะนำรีเอเจนต์การสกัดกรดนิวคลีอิกที่ผลิตโดย Dewei
ไม่จำเป็นต้องใช้การสกัดกรดนิวคลีอิกเมื่อใช้การควบคุมเชิงบวก การสกัดกรดนิวคลีอิกเป็นสิ่งจำเป็นเมื่อใช้การควบคุมเชิงลบ
[การจัดเก็บและความเสถียร]
ชุดอุปกรณ์สามารถเก็บไว้ที่อุณหภูมิ -20±5 ℃ ได้นาน 12 เดือน
เก็บชั่วคราวที่อุณหภูมิ 4 ℃ เป็นเวลา 7 วัน
การแช่แข็งและการละลายซ้ำไม่ควรเกิน 7 ครั้ง น้ำยาเปิดไม่ควรเกิน 7 ครั้ง
น้ำแข็งแห้งเพื่อให้ขนส่งที่อุณหภูมิต่ำไม่ควรเกิน 4 วัน
[เครื่องมือ]
เครื่องมือ PCR แบบเรียลไทม์ เช่น ABI7500, ABI7300, LightCycler480, Bio-Rad CFX96, SLAN-96S และ QuantStudio
[การสุ่มตัวอย่างและการจัดการ]
- ประเภทของสิ่งส่งตรวจที่เหมาะสม: ตัวอย่างซีรัมและรอยโรค
2. การรวบรวม: ควรเก็บตัวอย่างลงในหลอดปลอดเชื้อตามมาตรฐาน
ข้อกำหนดทางเทคนิค.
การเก็บรักษา: การเก็บตัวอย่างควรใช้สำหรับการตรวจจับทันทีหรือแช่แข็งที่
≤-20 °C ไม่เกินหนึ่งเดือน ควรหลีกเลี่ยงการแช่แข็งซ้ำและการละลาย
3. การขนส่ง: ตัวอย่างควรขนส่งโดยใช้กล่องโฟมปิดผนึกด้วยน้ำแข็ง
[มาตรการ]
- การบำบัดตัวอย่างและการสกัดกรดนิวคลีอิก (พื้นที่บำบัดตัวอย่าง)
ขอแนะนำให้เก็บตัวอย่างของเหลว 200μL การควบคุมเชิงบวก และการควบคุมเชิงลบสำหรับการสกัดกรดนิวคลีอิก ตามข้อกำหนดและขั้นตอนที่สอดคล้องกันของชุดการสกัดดีเอ็นเอของไวรัส
- การเตรียมรีเอเจนต์ PCR (พื้นที่เตรียมรีเอเจนต์)
ใส่หลอด PCR ลงในถังปฏิกิริยาและตั้งชื่อของแต่ละปฏิกิริยาให้ดีตามลำดับที่เกี่ยวข้อง
นำ MVP PCR Reagent A และ B ออกจากชุด ละลายที่อุณหภูมิห้อง เขย่าและผสม ปั่นเหวี่ยงที่ 8,000 รอบต่อนาทีเป็นเวลาสองสามวินาทีก่อนใช้งาน
ใช้หลอดปฏิกิริยา PCR N ชิ้น (N = จำนวนตัวอย่างที่จะทดสอบ + การควบคุมเชิงลบ + การควบคุมเชิงบวก)
การกำหนดค่าของระบบขยายสัญญาณเดียว MVP มีดังนี้:
| MPV PCR รีเอเจนต์ A |
17μL |
| MPV PCR รีเอเจนต์ B |
3μL |
| ระบบขยายเสียง |
20μL |
หลังจากผสมส่วนประกอบต่างๆ อย่างทั่วถึงแล้ว ให้ปั่นแยกเป็นเวลาสั้นๆ เพื่อให้ของเหลวทั้งหมดบนผนังท่อถูกหมุนเหวี่ยงไปที่ด้านล่างสุดของท่อ จากนั้นจึงจ่ายระบบขยายเสียง 20 µl ลงในหลอด PCR
- การเก็บตัวอย่าง (พื้นที่เตรียมตัวอย่าง)
เพิ่ม 5µl ของการควบคุมเชิงลบที่ประมวลผลแต่ละรายการ กรดนิวคลีอิกของตัวอย่างที่จะทดสอบ และการควบคุมเชิงบวก MVP ไปที่หลอด PCR ด้านบน ขันฝาท่อให้แน่นและหมุนเหวี่ยงที่ 8,000 รอบต่อนาทีเป็นเวลาสองสามวินาที จากนั้นโอนไปยังการตรวจจับการขยาย พื้นที่.
- การขยาย PCR (พื้นที่ขยาย)
ใส่หลอด PCR ลงในถังปฏิกิริยาและตั้งชื่อของแต่ละปฏิกิริยาให้ดีตามลำดับที่เกี่ยวข้อง
การตั้งค่าการตรวจจับเรืองแสง: (1) Monkeypox virus (FAM);(2) การควบคุมภายใน (CY5)
เรียกใช้โปรโตคอลการปั่นจักรยานต่อไปนี้: ABI7500, Bio-Rad CFX96, SLAN-96S และ QuantStudio โปรดดูคู่มือผู้ใช้เครื่องมือเพื่อการทำงานที่ดีขึ้น:
| |
ขั้นตอน |
อุณหภูมิ |
เวลา |
รอบ |
| 1 |
Pre-denaturation |
95 ℃ |
2นาที |
1 |
| 2 |
การเสื่อมสภาพ |
95 ℃ |
10 วิ |
45 |
| การหลอม การขยาย การได้มาซึ่งการเรืองแสง |
60 ℃ |
30 วิ |
- การวิเคราะห์ผลลัพธ์ (โปรดดูคู่มือผู้ใช้เครื่องมือ)
หลังจากเกิดปฏิกิริยา ผลลัพธ์จะถูกบันทึกโดยอัตโนมัติคลิก “วิเคราะห์” เพื่อวิเคราะห์ จากนั้นเครื่องมือจะแปลค่า Ct ของแต่ละตัวอย่างในคอลัมน์ผลลัพธ์โดยอัตโนมัติผลการควบคุมเชิงลบและบวกจะต้องเป็นไปตามต่อไปนี้
"5. การควบคุมคุณภาพ".
การควบคุมเชิงลบ: ไม่มี Ct หรือ Ct> 40 ในช่อง FAM, Ct≤40 ในช่อง CY5 พร้อมเส้นขยายปกติ
การควบคุมเชิงบวก: Ct≤35 ในช่อง FAM ที่มีเส้นขยายปกติ Ct≤40 ในช่อง CY5 ที่มีเส้นขยายปกติ
ผลลัพธ์จะถูกต้องหากตรงตามเกณฑ์ข้างต้นทั้งหมดมิฉะนั้น ผลลัพธ์จะไม่ถูกต้อง
[การตีความผลลัพธ์]
ผลลัพธ์ต่อไปนี้เป็นไปได้:
| |
ค่า Ct ของช่อง FAM |
ค่ากะรัตของช่อง CY5 |
การตีความ |
| 1# |
ไม่มีกะรัตหรือกะรัต>40 |
≤40 |
Monkeypox ไวรัสลบ |
| 2# |
≤40 |
ผลลัพธ์ใด ๆ |
Monkeypox ไวรัสบวก |
| 3# |
40~45 |
≤40 |
สอบใหม่;ถ้ายังคงเป็น 40~45 รายงานเป็น 1# |
| 4# |
ไม่มีกะรัตหรือกะรัต>40 |
ไม่มีกะรัตหรือกะรัต>40 |
ไม่ถูกต้อง |
หมายเหตุ: หากผลลัพธ์ที่ไม่ถูกต้องเกิดขึ้น จะต้องเก็บตัวอย่างและทดสอบอีกครั้ง
[ข้อจำกัดในการตรวจจับ]
ผลการตรวจจับของชุดนี้ใช้สำหรับการอ้างอิงทางคลินิกเท่านั้น และไม่ควรใช้เป็นหลักฐานในการวินิจฉัยและการรักษาทางคลินิกโดยตรงควรพิจารณาการจัดการทางคลินิกของผู้ป่วยร่วมกับอาการ ประวัติการรักษา และประวัติการสัมผัส
ผลการตรวจจับอาจได้รับผลกระทบจากการดำเนินการ รวมทั้งการเก็บตัวอย่าง การจัดเก็บ และการขนส่งผลลบที่เป็นเท็จอาจเกิดขึ้นหากมีข้อผิดพลาดในการดำเนินการการปนเปื้อนข้ามระหว่างการบำบัดสิ่งส่งตรวจอาจนำไปสู่ผลบวกที่ผิดพลาด
[ข้อมูลจำเพาะด้านประสิทธิภาพ]
ขีดจำกัดการตรวจจับ: 500 สำเนา/มล.
ความแม่นยำ: ค่าสัมประสิทธิ์การแปรผัน (CV, %) ของค่า Ct ภายในชุด/ระหว่างชุดความแม่นยำคือ ≤5%
ความแม่นยำ: อัตราความสอดคล้องของการอ้างอิงเชิงลบ/บวก: 100%
ความจำเพาะ: ไม่มีปฏิกิริยาข้ามกับจีโนมมนุษย์และเชื้อโรคต่อไปนี้: ไวรัสไข้ทรพิษ, ไวรัสอีสุกอีใส, ไวรัสวัคซีน, ไวรัสอีสุกอีใส, ไวรัสตับอักเสบบี, ไวรัสตับอักเสบซี, ไวรัสภูมิคุ้มกันบกพร่องของมนุษย์, enterovirus
[ข้อควรระวัง]
- ผลิตภัณฑ์นี้ใช้สำหรับการทดสอบในหลอดทดลองเท่านั้นโปรดอ่านคู่มือนี้อย่างละเอียดก่อนใช้งาน
- ใช้หลอดและคำแนะนำที่ปราศจากเชื้อ ปราศจาก DNase และ RNase ระหว่างการตรวจจับ
- ระหว่างการตรวจจับ จำเป็นต้องหลีกเลี่ยงการปนเปื้อนข้าม สวมอุปกรณ์ป้องกันที่เหมาะสม ถุงมือและหน้ากากแบบใช้แล้วทิ้ง และดำเนินการในตู้ความปลอดภัยทางชีวภาพให้เสร็จสิ้นเพื่อหลีกเลี่ยงสารอันตรายเข้าสู่ทางเดินหายใจ
- ในกรณีที่สัมผัสกับผิวหนังและเยื่อเมือกระหว่างการใช้งาน โปรดล้างออกทันทีด้วยน้ำไหล ซึ่งจะไม่เป็นอันตรายต่อผู้ปฏิบัติงาน
รีเอเจนต์เหลวทั้งหมดควรละลายจนหมดและผสมที่อุณหภูมิห้องก่อนใช้งาน และปั่นเหวี่ยงที่ 8,000 รอบต่อนาทีเป็นเวลาสองสามวินาทีก่อนใช้งาน
หลังการใช้งาน บรรจุภัณฑ์และของเสียของเหลวต้องได้รับการปฏิบัติอย่างสม่ำเสมอเหมือนของเสียทางการแพทย์ เพื่อป้องกันมลพิษ

 ข้อความของคุณจะต้องอยู่ระหว่าง 20-3,000 ตัวอักษร!
ข้อความของคุณจะต้องอยู่ระหว่าง 20-3,000 ตัวอักษร! กรุณาตรวจสอบอีเมลของคุณ!
กรุณาตรวจสอบอีเมลของคุณ!  ข้อความของคุณจะต้องอยู่ระหว่าง 20-3,000 ตัวอักษร!
ข้อความของคุณจะต้องอยู่ระหว่าง 20-3,000 ตัวอักษร! กรุณาตรวจสอบอีเมลของคุณ!
กรุณาตรวจสอบอีเมลของคุณ!